バイオテクノロジーに関連する気になるカタログにチェックを入れると、まとめてダウンロードいただけます。
再生医療製品の法務支援とは?課題と対策・製品を解説

目的・課題で絞り込む
医薬・創薬
カテゴリで絞り込む
アカデミア/公的研究機関 |
医療・創薬 |
医療/診断/医療機器 |
化成品/化粧品 |
環境/エネルギー |
研究用機器・試薬・消耗品/設備 |
食品/農林水産/畜産 |
創薬支援/受託サービス |
知的財産/法務/金融 |
その他バイオテクノロジー |

医薬・創薬における再生医療製品の法務支援とは?
各社の製品
絞り込み条件:
▼チェックした製品のカタログをダウンロード
一度にダウンロードできるカタログは20件までです。
【医薬品向け】FTA/EPAを活用したコスト削減
【製薬業界向け】高調波診断ツール
【製薬会社向け】ネットワーク|ソリューション部
【製薬工場向け】AiPicsによる害虫管理の効率化
【製薬会社向け】SAFプログラムによるCO2排出量削減
【CRO向け】CNSCシリーズ
【バイオテクノロジー向け】CNSCシリーズ
【医療機器向け】ステンレスメッシュフィルター
【製薬会社向け】廃棄薬品・試験研究廃液の処理
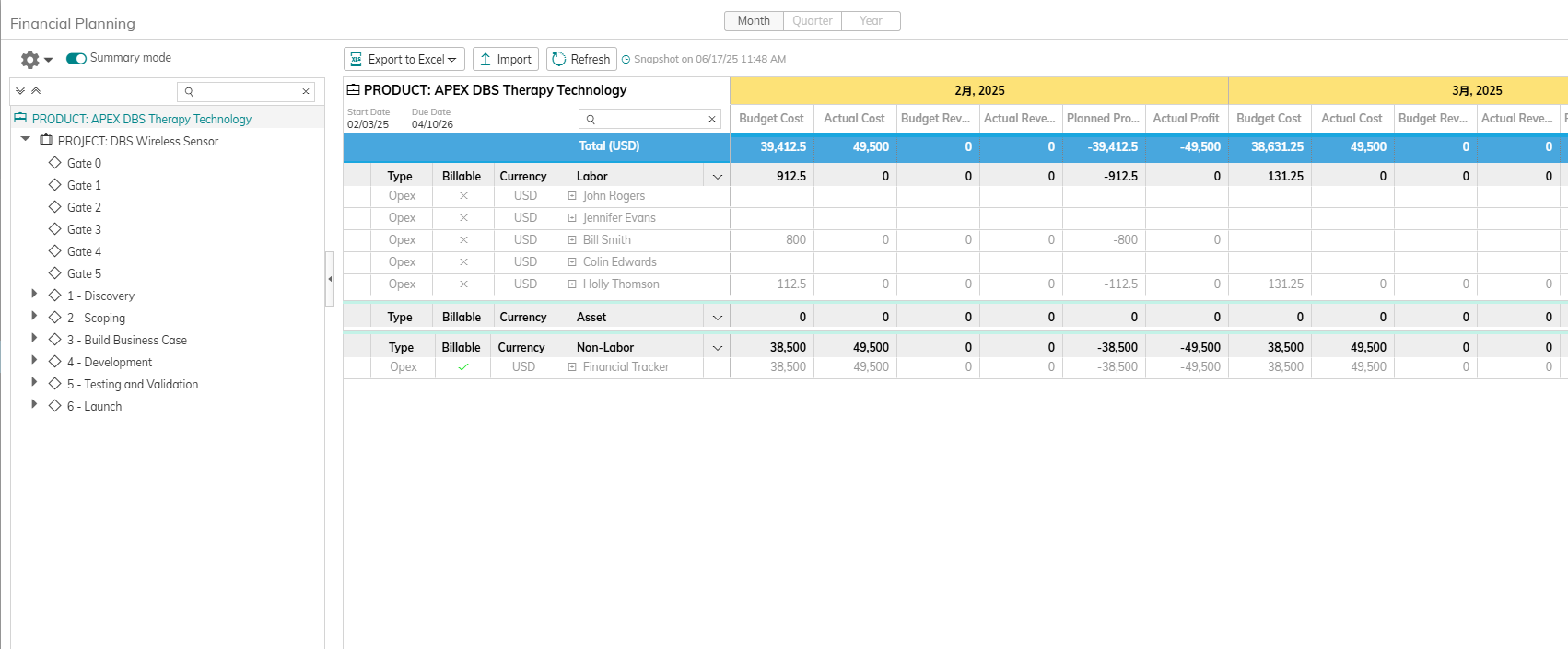
【製薬業界向け】AdaptiveWorkでプロジェクト財務管理
【医療機器向け】PERFREZ O-リング
【大学研究機関向け】『 契印機 』・『 ��打抜機 』
【医療関連設備向け】PFA樹脂製フローサイト 研究設備用配管
【医療機器向け】DMA 動的粘弾性測定
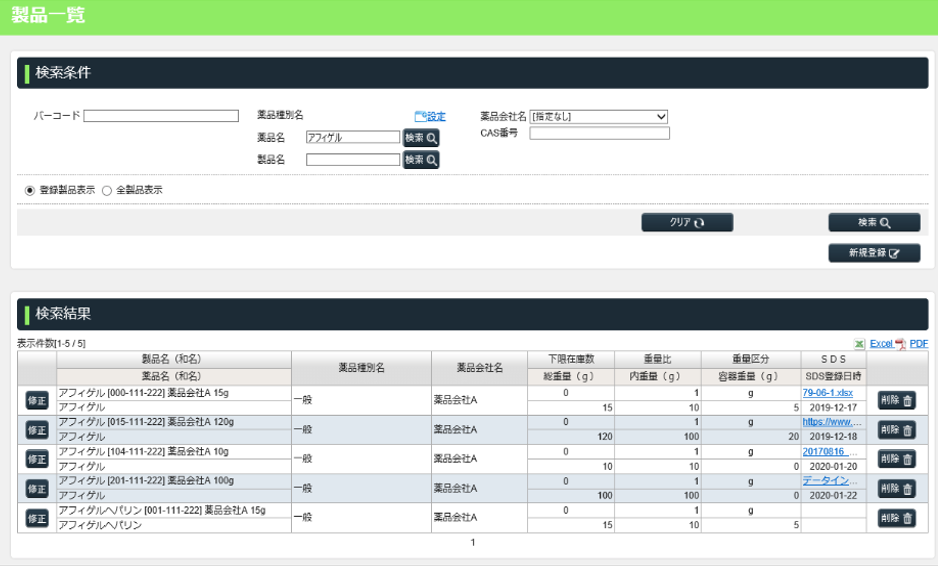
薬品に関する多くの情報を登録可能
薬事コンプライアンス支援サービス
製造委受託支援サービス
BIO IT SERVICE 会社案内
マイコプラズマ遺伝子検出キット『Myco Finder』
化学物質管理支援サービス
迅速マイコプラズマ否定試験サービス
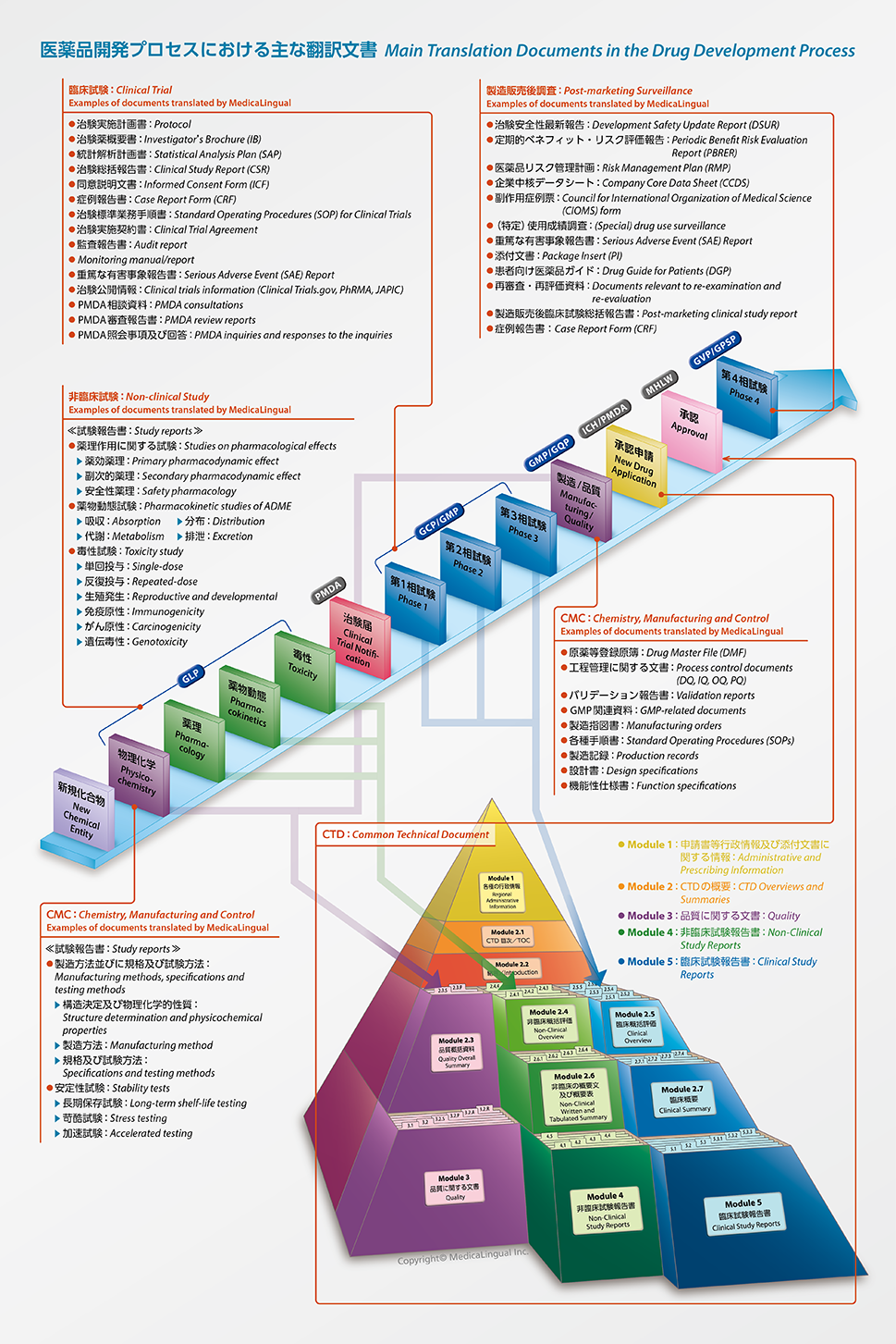
医薬翻訳サービス
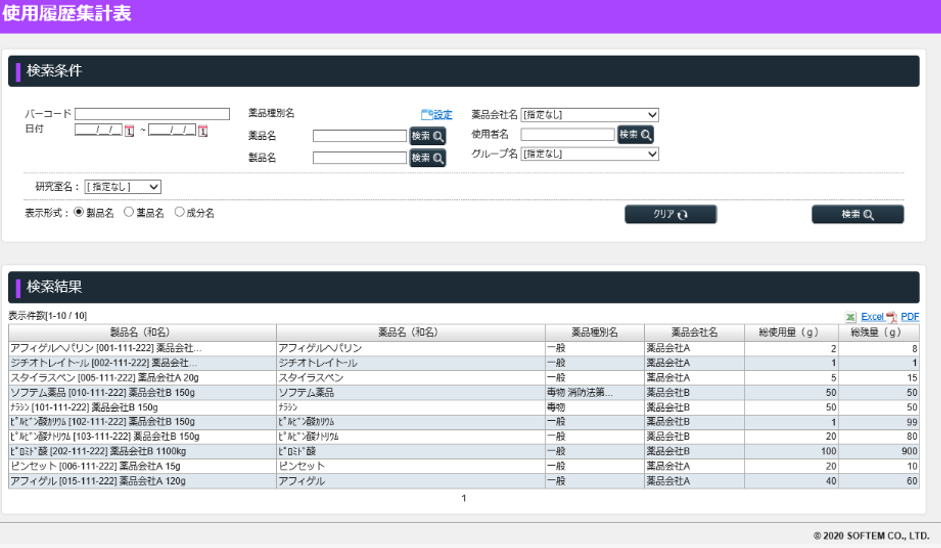
管理がずっと楽になる集計機能
1.薬事コンサルタント2.海外医療機器の輸入・保管等のお悩み解決
医薬翻訳サービス
医薬品・医療機器業界向け コンサルディングサービス
メディカルサイエンス 編集・出版サービス
規制関連業務(承認申請対応など)
大杉バイオファーマ・コン��サルティング株式会社 事業紹介
薬事戦略・開発戦略 コンサルティングサービス
【メディカルライティング】薬事申請関連文書ライティング
再生医療支援サービス
調査レポート『国内再生医療等製品 受託開発調査』CDMO/CMO
翻訳サービス
ホルマリン希釈装置
試薬ライン『SFC-5』
薬事コンサルティングサービス

お探しの製品は見つかりませんでした。
1 / 1
医薬・創薬における再生医療製品の法務支援
医薬・創薬における再生医療製品の法務支援とは?
再生医療製品の開発・製造・販売に関わる法的な課題に対し、専門的な知識と経験に基づいた助言やサポートを提供するサービスです。規制当局との折衝、知的財産権の保護、契約交渉、コンプライアンス体制の構築などを包括的に支援し、製品の実用化と事業の安定化を目指します。
課題
複雑化する規制への対応
再生医療分野は、各国で法規制が急速に変化・整備されており、最新の規制動向を把握し、遵守することが困難です。
知的財産権の保護と活用
革新的な技術や細胞株、治療法に関する権利を適切に保護し、将来的なライセンス契約や共同開発に繋げることが重要ですが、その戦略立案と実行が課題となります。
倫理的・社会的な課題への配慮
ヒト由来の細胞や組織を用いるため、インフォームド・コンセント、個人情報保護、遺伝子操作に関する倫理的な問題や社会的な受容性への対応が求められます。
国際的な事業展開における法規制の差異
グローバル市場を目指す場合、各国の薬事法、製造販売承認プロセス、データ保護規制などの違いを理解し、統一的な戦略を立てることが複雑な課題となります。
対策
規制当局との連携強化
早期段階から規制当局との積極的なコミュニケーションを図り、承認プロセスに関する情報収集と助言を得ることで、円滑な開発を促進します。
包括的な知財戦略の策定
特許出願、営業秘密管理、共同研究開発契約における知財条項の精査など、製品ライフサイクル全体を見据えた知財戦略を構築・実行します。
コンプライアンス体制の構築支援
GxP(医薬品の製造管理及び品質管理に関する基準)遵守、個人情報保護法、倫理指針等に基づいた社内規程の整備や教育プログラムの提供を行います。
国際法務アドバイスと契約支援
海外の法規制専門家との連携により、各国の薬事申請、臨床試験、販売契約に関する法的なアドバイスと契約書作成・交渉を支援します。
対策に役立つ製品例
規制コンサルティングシステム
最新の薬事規制情報、承認事例、当局との質疑応答記録などを集約し、企業が迅速かつ正確に規制要�件を理解・対応できるよう支援します。
知的財産管理・分析システム
特許ポートフォリオの管理、競合他社の知財動向分析、権利侵害リスク評価などを自動化・効率化し、戦略的な知財活用をサポートします。
契約書レビュー・作成支援ツール
再生医療分野に特化した契約書テンプレートや、AIによる契約書レビュー機能を提供し、契約締結までの時間短縮とリスク低減を実�現します。
グローバル薬事申請サポートサービス
各国の薬事申請書類作成支援、現地コンサルタントとの連携、申請状況の進捗管理など、国際的な承認取得プロセスを包括的に支援します。
⭐今週のピックアップ

読み込み中